Kupfer(I)-bromid ist ein Kupfersalz des Bromwasserstoffs mit der Verhältnisformel CuBr. Kupfer besitzt hierbei die Oxidationsstufe 1.
Darstellung
Kupfer(I)-bromid kann durch die Reaktion elementaren Kupfers mit Bromwasserstoffsäure hergestellt werden. Dazu wird elementares Kupfer mit einer etherischen Lösung von HBr umgesetzt und das entstehende HCuBr2 mit Waser zersetzt
Eine weitere Synthesemöglichkeit besteht in der Reduktion von Kupfer(II)-bromid. Als Reduktionsmittel können beispielsweise Sulfitverbindungen dienen.
Diese Reduktion kann auch beim Kochen des Kupfer(II)-bromids in saurer Lösung mit einem Überschuss an Kupfer erfolgen.
Ebenfalls möglich ist die Synthese durch Reaktion von Kupfersulfat-Pentahydrat mit Kaliumbromid und Schwefeldioxid.
Eigenschaften
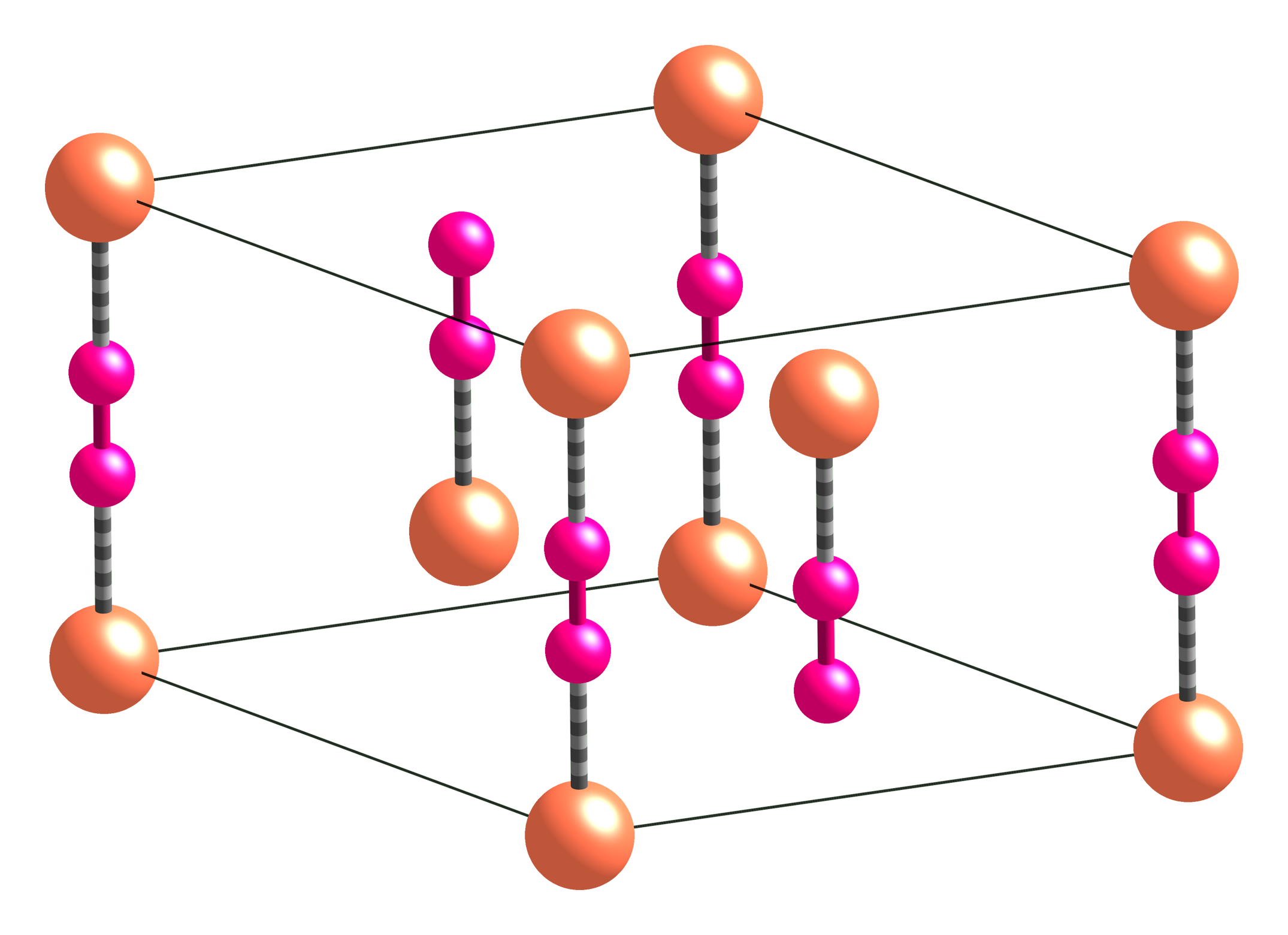
Das eigentliche Salz ist farblos. Seine grünliche Farbe erhält es durch Verunreinigungen mit Kupfer(II)-Ionen. Kupfer(I)-bromid ist unlöslich in den meisten Lösungsmitteln. Es ist schwerlöslich in Wasser, aber löslich in Halogenwasserstoffsäuren, Salpetersäure und wässrigem Ammoniak. Kupfer(I)-bromid tritt in drei Modifikationen auf. Unterhalb von 391 °C liegt es als γ-CuBr mit einer Kristallstruktur vom Zinkblende-Typ und der Raumgruppe F43m (Raumgruppen-Nr. 216)Vorlage:Raumgruppe/216 (a = 5,691 Å) vor. β-CuBr mit einer Kristallstruktur vom Wurtzit-Typ liegt zwischen 391 °C und 470 °C vor. α-CuBr mit einer kubischen Kristallstruktur oberhalb 470 °C.
Verwendung
Ein Einsatzgebiet von Kupfer(I)-bromid ist die Sandmeyer-Reaktion. Hier wird es als Katalysator zur Synthese von Arylbromiden aus Arylaminen über die entsprechenden Diazoniumsalze eingesetzt. Bei thermischer Anregung erzeugt gasförmiges Kupfer(I)-bromid blaues Licht, das eine höhere Farbsättigung aufweist als das durch Kupfer(I)-chlorid emittierte Licht. Kupfer(I)-bromid ist daher ein geeigneter Emitter für pyrotechnische Leuchtsätze.
Literatur
- Wiberg, E.; Wiberg, N.; Holleman, A.F.: Anorganische Chemie, 103. Auflage, 2017 Walter de Gruyter GmbH & Co. KG, Berlin/Boston, ISBN 978-3-11-026932-1, S. 1696.
Einzelnachweise